2026年2月,科望医药自主研发的全球首创CD39/TGF-β双特异性抗体ES014,正式获得美国FDA授予的孤儿药资格认定,用于治疗硬纤维瘤。这一里程碑事件,不仅是国际监管机构对ES014临床价值与创新机制的权威认可,更将全面加速产品全球临床开发与商业化进程,显著提升公司创新管线的全球商业价值,为科望医药全球化战略布局注入强劲动力。
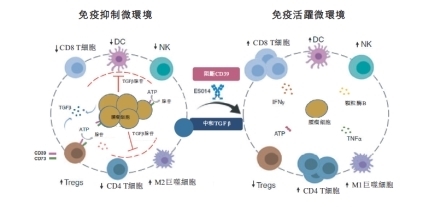
图:ES014作用机制
作为全球首个进入临床阶段的CD39/TGF-β双抗,ES014的核心创新在于同时靶向肿瘤微环境中CD39-腺苷通路和TGF-β通路两大关键免疫抑制通路,既能解除腺苷通路介导的免疫抑制,又能阻断TGF-β通路带来的肿瘤微环境免疫耐受,通过双重机制协同起效重塑肿瘤免疫微环境,发挥抗肿瘤活性。其Ⅰ期临床数据显示,ES014在硬纤维瘤患者队列中客观缓解率(ORR)达40%,疾病控制率(DCR)实现100%,且整体安全性特征良好,未观察到剂量限制性毒性,大多数治疗相关不良事件为轻度,为硬纤维瘤这一罕见病患者提供了全新、更安全的治疗选择。
根据FDA《孤儿药法案》相关政策,此次资格认定为ES014带来多重研发与商业化红利,核心包括获批上市后长达7年的美国市场独占权、临床试验费用税费抵免、免除新药上市申请(NDA/BLA)费用,以及FDA在开发过程中更为密切的审评指导等多方面支持。上述政策可能大幅缩短ES014的全球临床开发周期,显著降低研发成本、提升商业化确定性,为产品快速登陆全球市场铺平道路,同时为后续其他适应症的全球开发奠定基础。
从行业视角来看,FDA孤儿药资格认定是中国创新药出海的核心通行证之一,也是全球医药市场对创新药临床价值的核心评判标准。科望医药ES014此次斩获认定,不仅为硬纤维瘤患者带来了全新的治疗希望,更印证了中国原创生物药的全球创新实力。在全球创新药竞争日趋激烈的背景下,科望医药凭借源头创新的技术平台与清晰的全球化开发路径,正持续为中国创新药出海打造标杆案例,其后续管线的全球临床进展与商业化布局值得持续关注。
(责任编辑:华康)